-
서울대병원 연구팀이 동물의 심장판막 조직에서 면역 거부반응의 원인이 되는 항원을 제거하고, 사람 세포를 다시 심어 살아 있는 조직처럼 만드는 데 성공했다.
체외(體外) 환경에서 이종 조직의 재세포화(Recellularization) 가능성을 입증한 이번 연구는, 성장기 어린이 환자에게 반복적으로 필요한 심장판막 교체 수술의 부담을 줄일 수 있는 차세대 이식재 개발의 기초 근거로 평가된다.
현재 심장 수술에서는 돼지나 소의 심낭 및 판막 조직이 이식재로 널리 사용된다. 하지만 사람에게 없는 α-Gal과 Neu5Gc 같은 이종항원이 남아 있어 인체 내에서 면역 거부반응을 일으키며 염증, 석회화, 조직 손상 등을 유발할 수 있다. 특히 소아 환자의 경우 성장 과정에서 이식된 판막이 함께 발달하지 않아 5~10년마다 재수술받아야 하는 사례도 적지 않다.
이 때문에 면역 거부를 줄이면서도 인체 세포가 안정적으로 정착할 수 있는 새로운 이식재 기술이 오랫동안 과제로 제시됐다.
서울대병원 의생명연구원 김소영 연구교수, 소아청소년과 김기범 교수, 소아흉부외과 임홍국 교수 연구팀은 돼지 심장판막에서 기존 세포를 제거하는 ‘탈세포화(Decellularization)’를 진행한 뒤, α-갈락토시다아제(α-Gal 제거)와 PNGase-F(Neu5Gc 제거)를 함께 처리해 이종항원을 없앴다.
이후 사람 지방유래 중간엽 줄기세포(ADSCs)와 제대정맥 내피세포(HUVECs)를 공배양하여 재세포화 과정을 관찰했다. ‘재세포화’란 탈세포화된 생체 조직의 기질에 환자 세포를 다시 심어 살아 있는 조직처럼 기능하도록 만드는 기술이다.
-
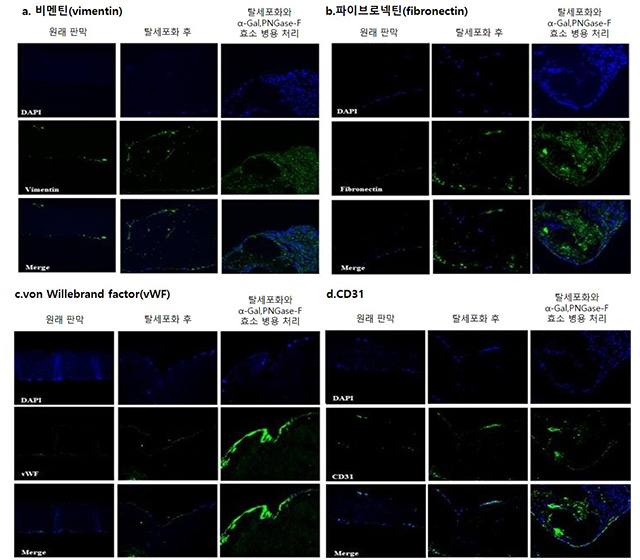
연구 결과, 두 효소를 병용했을 때 판막의 구조와 강도는 유지되면서 항원 제거 효과가 크게 향상됐다. 또 공배양된 세포가 조직 내부로 침투해 자리를 잡았고, 비멘틴(Vimentin), 파이브로넥틴(Fibronectin), 폰빌레브란트 인자(vWF), CD31 등 세포 정착 및 내피 형성과 관련된 단백질 발현이 증가했다.
연구팀은 이를 ▲조직 안정성 유지 ▲주요 항원 제거 ▲탄수화물 결합 렉틴 신호 감소 등 세 가지 효과가 동시에 관찰된 결과로 설명했다.
임홍국 교수(소아흉부외과)는 “항원 제거 효율을 높인 뒤 사람 세포를 공배양해 체외에서 재세포화 반응을 확인했다”며 “향후 동물실험과 임상연구를 통해 실제 적용 가능성을 검증할 계획”이라고 말했다.
이번 연구는 이건희 소아암·희귀질환 극복 사업의 지원으로 수행됐으며, 결과는 재생의학 분야 국제학술지 Tissue Engineering: Part A 온라인판에 게재됐다.
서울대병원 연구팀은 앞서 2018년 자체 개발한 항석회화 프로토콜을 돼지 심낭에 적용해 폐동맥 스텐트 판막을 개발한 바 있다. 이 판막은 현재까지 872명의 환자에게 이식돼 우수한 임상 결과를 보였으며, 이번 연구는 그 기술적 기반을 확장해 ‘거부반응을 최소화한 생체 기반 판막’ 개발로 이어질 가능성을 제시했다.
- 김정아 기자 jungya@chosun.com