-
강스템바이오텍이 7일 서울 여의도 전경련 컨퍼런스센터에서 개최한 기업설명회에서 현재 진행 중인 아토피 치료제 ‘퓨어스템-에이디주’ 임상 3상의 1년 시점 장기추적 데이터를 발표했다.
-
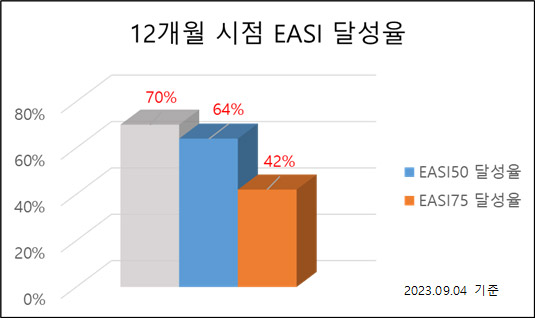
공개된 자료에 따르면 퓨어스템-에이디주는 투약 후 1년 시점의 EASI50 달성률은 최소 64%에서 최대 70%로, 지난해 발표한 2019년 임상 3상에 대한 장기추적조사(K0102-E) 결과인 58% 대비 10~20% 향상률을 확인했다. 또한, 제품 경쟁력 제고를 위해 추가로 확인한 EASI75 달성률의 경우 42%로 시판 중인 항체치료제 수준의 추세를 보였다.
-
사측은 현재 이번 임상 3상에 대한 장기추적조사가 진행 중이라며, 추후 포함될 환자 수 및 현재 데이터 추세를 고려했을 때 1년 시점에서 최대 70%까지 EASI50를 달성할 것으로 예상했다.
배요한 임상개발본부장은 “장기적 효능을 감안했을 때 이번 임상 3상의 결과를 확인하는 시점인 12주 차의 데이터 또한 긍정적일 것으로 기대되며, 임상 현장에서 빠른 개선에 대한 긍정적인 평가를 받는 등 지난 1차 임상 3상과 확연한 차이를 보여 임상 결과에 대한 기대감이 높다”며, “EASI75 달성률도 2018년 출시 이후 급격한 매출 성장을 보이는 항체치료제 수준인 42%로 나타나 약물 경쟁력 또한 향상될 것으로 보인다”고 말했다.
이날 기업설명회에서는 임상 1상 투약을 진행 중인 골관절염 치료제에 대한 발표도 진행됐다.
8월 초 임상 1상에 돌입해 최근 저용량군에 대한 투약을 마친 퓨어스템-오에이 키트주는 이상 반응이 나타나지 않으며 연내 1상 투약을 완료하고 내년 상반기에 약물의 6개월간 안전성 및 MRI 기반 영상 데이터 판독을 통한 연골의 구조적 개선을 확인할 계획이다. 사측은 동물시험에서 확보한 연골조직 재생, 연하골 구조개선이 인체에서도 확인될 경우 2024년 내 라이선스 아웃이 가능할 것으로 예견했다.
강스템바이오텍은 내년 상반기 퓨어스템-에이디주 임상 3상 데이터를 확보하면, 하반기에 식약처 품목허가를 신청할 예정이다.
나종천 대표는 “아토피 및 골관절염 치료제의 임상 결과가 가시화되면서 줄기세포 치료제 개발 기업으로서 중차대한 시점을 맞이했다. 많은 분의 기대와 성원에 힘입어 조속히 줄기세포 치료제의 품목허가 및 기술수출 등 사업 성과를 이룰 수 있도록 노력하겠다”고 말했다.
- 김정아 기자 jungya@chosun.com