-
㈜종근당이 제조한 9개 의약품이 ‘약사법’을 위반한 것으로 드러나 제조·판매가 잠정 중지됐다.
식품의약품안전처(이하 식약처)는 ‘의약품 GMP 특별 기획점검단’이 지난 4월 5일부터 실시한 의약품 제조업체 4개에 대한 특별 불시 점검 결과, ㈜종근당에서 제조(수탁 제조 포함)한 9개 의약품이 ‘약사법’을 위반한 것으로 확인했다고 밝혔다. 해당 제품의 위반 사항은 ▲변경허가를 받지 않고 첨가제 임의 사용, ▲제조기록서 거짓 이중작성·폐기, ▲제조 방법 미변경, ▲원료 사용량 임의 증감 등이었으며, 식약처는 9개 의약품에 대해 잠정 제조·판매 중지 등을 조치했다.
-
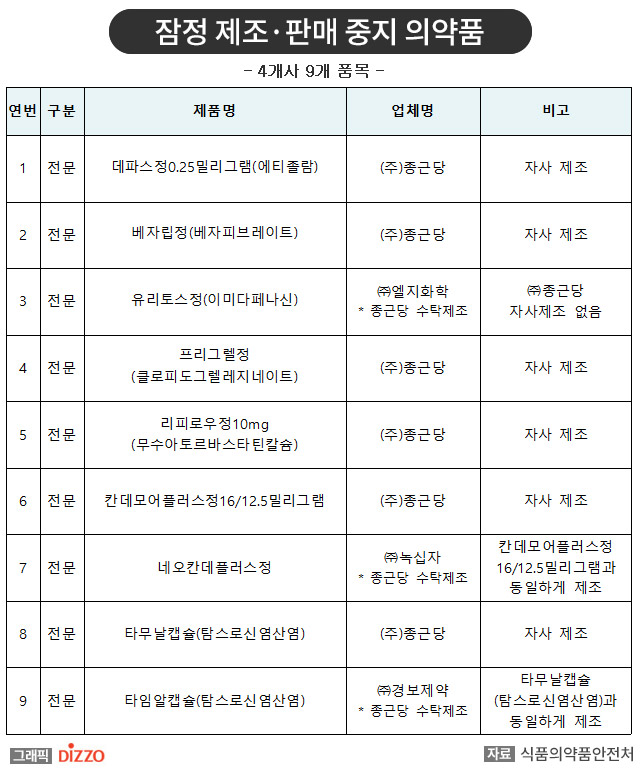
이번 잠정 제조·판매 중지된 9개 의약품은 ▲데파스정0.25밀리그램, ▲베자립정, ▲유리토스정, ▲프리그렐정, ▲리피로우정10mg, ▲칸데모어플러스정16/12.5밀리그램, ▲네오칸데플러스정, ▲타무날캡슐, ▲타임알캡슐이다.
이 중 4개 품목(데파스정0.25밀리그램, 베자립정, 유리토스정, 프리그렐정)은 ‘공급 중단 보고대상 의약품’이다. 식약처는 ▲의료상 다른 의약품으로 대체가 어려운 점 ▲수거·검사한 결과 함량 등은 시험기준 내에 있다는 점 등을 고려해 중앙약사심의위원회 전문가 자문 의견 등을 종합적으로 검토해 환자 치료상 필요성 등이 인정되는 3개 품목(데파스정0.25밀리그램, 베자립정, 유리토스정)은 잠정 제조·판매 중지 조치는 적용하되, 시중 유통제품 사용은 허용하기로 했다.
그 외 6개 품목(리피로우정10mg, 칸데모어플러스정16/12.5밀리그램, 네오칸데플러스정, 타무날캡슐, 타임알캡슐, 프리그렐정)은 다른 대체 의약품으로 전환 및 제품 회수가 수행될 수 있도록 의·약사 등 전문가에게 협조를 요청하는 안전성 속보를 배포하고, 보건복지부 및 건강보험심사평가원을 통해 병·의원 등에 해당 품목의 처방이 제한되도록 요청했다.
식약처는 앞으로도 ‘의약품 GMP 특별 기획점검단’의 의약품 제조소 불시 점검을 연중 실시하고 그 결과는 투명하게 공개하며, 환자 안전을 최우선으로 고려하여 신속하게 필요한 조치를 해나가겠다고 밝혔다. 아울러 고의적 제조 방법 임의변경 제조, 허위·이중 기록 작성 등 위법 행위에 대해서는 GMP 적합판정을 취소하고, 해당 위반행위를 통해 얻은 부당한 이익에 대해 징벌적 과징금을 부과하도록 ‘약사법’ 개정 등을 추진할 계획이다.
- 김정아 기자 jungya@chosun.com